MicroRNA Containing iPS Cell–Derived Exosomes May Enable a Japanese Person to ‘Transform’ Into an American
“TIMC’s Dr. Fukutomi Becomes the First in the World to Propose That MicroRNA Containing iPS Cell–Derived Exosomes May Enable a Japanese Person to ‘Transform’ Into an American”
<A New Hypothesis Suggesting Reactivation of Early Embryonic Genetic Programs>
Dr.Fukutomi of TIMC has announced a novel hypothesis suggesting that microRNAs contained in iPS cell–derived exosomes may influence physical traits in adults. The hypothesis proposes that genetic regulatory programs normally active only in the early human embryo may be reactivated by exosome administration, offering a new perspective on phenotypic change.
In human development, embryonic stem cells (ES cells) arise from the inner cell mass (ICM) of the blastocyst between days 4 and 7 after fertilization. During this period, these cells release extracellular vesicles (EVs) containing diverse microRNAs known to influence gene expression in the cell populations that will form the fetus.
TIMC focused on the fact that iPS cell–derived exosomes possess microRNA profiles similar to those of ES cell derived EVs. The institute suggests that when administered to adult tissues, these exosomes may partially reactivate genetic regulatory networks characteristic of the early embryo.
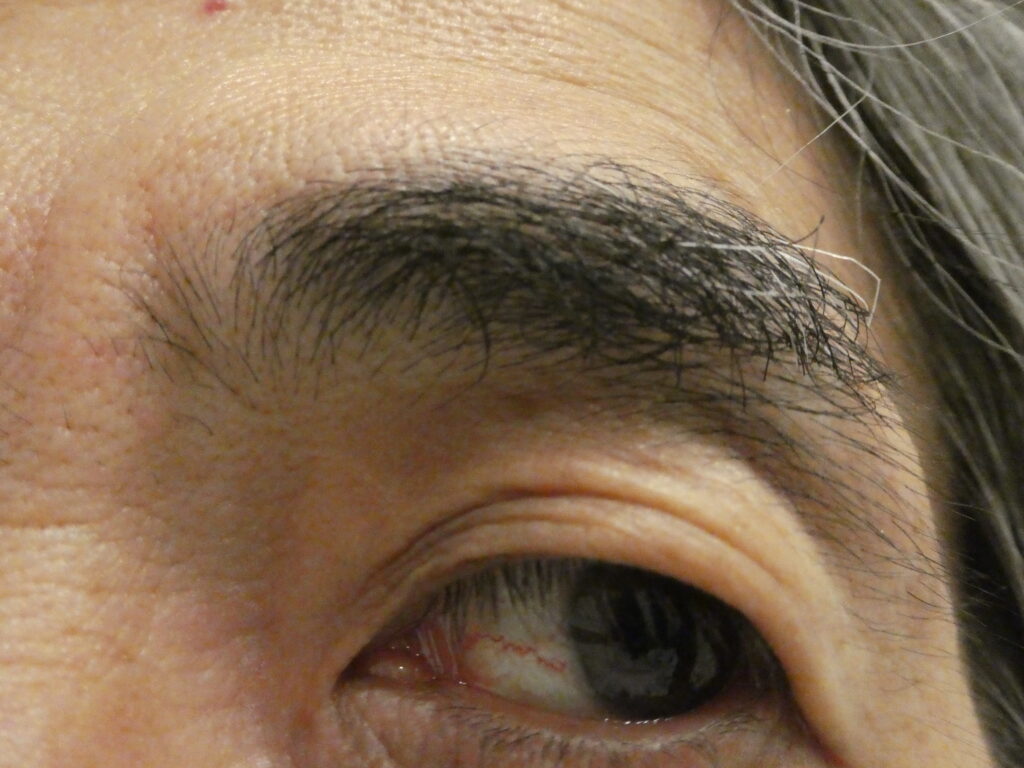
Dr. Fukutomi reports that after administering iPS cell–derived exosomes to himself, his eyelids changed from monolid to double eyelids within approximately one month. He explains that this phenomenon may reflect the reactivation of developmental programs in tissues such as the eyelid skin, the levator palpebrae superioris muscle, and the levator aponeurosis.
Double eyelids are common among Caucasians and less common among Japanese individuals, yet the relevant genes exist in the Japanese genome as well. Dr. Fukutomi suggests that a dormant “phenotype forming program” within the cells may have been “restored,” allowing latent traits to emerge.
He characterizes the phenomenon not as “rejuvenation” but as phenotypic reprogramming. The process may mirror the genetic regulation that occurs during the blastocyst stage (days 4–7 after fertilization), implying that similar molecular mechanisms could have been reactivated in adult tissues.
While the possibility that iPS cell–derived exosomes can influence adult phenotypes presents a potentially new application in regenerative medicine, further scientific validation remains necessary.
【 MicroRNA! What Is It? — April 6, 2026 】
▼ Medical Textbook Version
Phenotypic Change Induced by MicroRNA Containing iPS Cell–Derived Exosomes: The TIMC Hypothesis
During early human development, the morula forms around day 4 after fertilization, followed by blastocyst formation on days 5–6. The blastocyst contains an inner cell mass (ICM), from which embryonic stem cells (ES cells) are derived. ES cells begin to lose pluripotency as implantation starts around day 7.
During this period, the ICM and surrounding extraembryonic tissues release extracellular vesicles (EVs) containing diverse microRNAs. These microRNAs are believed to regulate gene expression in early embryonic cells and influence subsequent morphogenesis and organogenesis. Thus, microRNAs in ES cell derived EVs during days 4–7 may contribute to human phenotype formation by acting on the gene expression networks of cells destined to become the fetus.
iPS cell–derived exosomes have been reported to possess microRNA profiles similar to those of ES cell derived EVs and may mimic the gene regulatory effects characteristic of undifferentiated cells.
Dr. Fukutomi reports that after beginning self administration of iPS cell–derived exosomes, his eyelids changed from monolid to double eyelids within approximately one month. The TIMC hypothesis proposes that microRNAs in these exosomes may have reactivated portions of developmental programs in tissues such as the eyelid skin, the levator muscle, and the levator aponeurosis.
Although double eyelids are more common among Caucasians, the genes involved in double eyelid formation are also present in the Japanese genome. The TIMC hypothesis likens the latent “phenotype forming program” within cells to a computer’s recovery function, suggesting that microRNAs in iPS derived exosomes may have re initiated this program.
The hypothesis interprets the eyelid change not as rejuvenation but as re activation of phenotype determining processes normally occurring during the blastocyst stage. In other words, molecular mechanisms similar to those by which ES cell derived EVs influence ICM gene expression during days 4–7 after fertilization may have occurred again in adult tissues.
This hypothesis proposes that iPS cell–derived exosomes may reactivate portions of developmental programs in adult tissues, raising the possibility of phenotypic reprogramming beyond conventional rejuvenation.
【 TIMC microRNA News EVs — April 6, 2026 】
【マイクロRNA含有iPS細胞由来エクソソームで日本人がアメリカ人に生まれ変われる可能性をTIMCの福富氏が世界で初めて発見】
<初期胚プログラム再活性化の可能性を示す新仮説>
TIMCの福富氏は、iPS細胞由来エクソソームに含まれるマイクロRNAが、成人の身体的特徴に影響を与える可能性を示す独自の仮説を発表した。初期胚で働く遺伝子制御プログラムが、エクソソーム投与によって再び作動する可能性を指摘しており、形質変化に関する新たな視点として注目されている。
ヒトの発生では、受精後4〜7日の胚盤胞期に、内部細胞塊(ICM)から胚性幹細胞(ES細胞)が生じる。この時期の細胞はマイクロRNAを含むエクストラセルラー・ベジクル(EVs)を放出し、胎児となる細胞群の遺伝子発現に影響を与えることが知られている。
TIMCは、iPS細胞由来エクソソームがES細胞由来EVsと類似したマイクロRNAプロファイルを持つ点に着目。成人組織に投与した場合、初期胚で働く遺伝子制御ネットワークの一部が再活性化する可能性を示した。
TIMCの福富氏は、自身にiPS細胞由来エクソソームを投与したところ、約1か月後に一重瞼から二重瞼へと変化したと報告している。福富氏はこの現象について、「眼瞼皮膚や挙筋腱膜付着部などの組織に、発生学的プログラムの再作動が起きた可能性がある」と説明する。
二重瞼は白人に多く、日本人では比較的少ないが、関連遺伝子は日本人にも存在する。福富氏は、細胞内に眠る形質形成プログラムが“復元”されることで、潜在的な形質が発現した可能性を示唆した。
福富氏は今回の現象を「若返り」ではなく、「形質再構築(phenotypic reprogramming)」と位置づける。受精後4〜7日の胚盤胞期に起こる遺伝子制御と類似した作用が、成人組織で再現された可能性があるという。
iPS細胞由来エクソソームが成人の形質に影響を与える可能性は、再生医療の新たな応用領域として期待される一方、科学的検証は今後の課題となる。
【マイクロRNA!はて? 2026年4月6日】
▼医学書用の解説
【マイクロRNA含有 iPS細胞由来エクソソーム投与による形質変化の可能性:TIMC仮説】
ヒトの初期発生において、受精後約4日で桑実胚が形成され、続いて5〜6日目には胚盤胞が成立する。胚盤胞内部には内部細胞塊(inner cell mass:ICM)が存在し、この細胞群から胚性幹細胞(embryonic stem cells:ES細胞)が樹立される。
ES細胞は受精後7日目前後に始まる着床過程に伴い分化を開始し、未分化性を失う。
この時期の胚では、ICMおよび周囲の胚外組織からエクストラセルラー・ベジクル(EVs)が放出される。これらのEVsには多様なマイクロRNAが含まれ、初期胚の遺伝子発現制御に関与し、将来の形態形成や器官発生に影響を与えると考えられている。
すなわち、受精後4〜7日の期間における胚性幹細胞由来EVsのマイクロRNAは、胎児となる細胞群の遺伝子発現ネットワークに作用し、ヒトの形質形成に寄与する可能性がある。
iPS細胞由来エクソソームは、ES細胞由来EVsと類似したマイクロRNAプロファイルを持つことが報告されており、未分化細胞特有の遺伝子制御作用を模倣しうると考えられる。
TIMCの福富氏は、自身にiPS細胞由来エクソソームの投与を開始したところ、約1か月後に眼瞼が一重瞼から二重瞼へと変化したと報告している。
この現象についてTIMC仮説では、眼瞼皮膚、眼瞼挙筋、挙筋腱膜付着部などの組織に対し、エクソソームに含まれるマイクロRNAが発生学的プログラムの一部を再活性化させた可能性を指摘している。
二重瞼は白人に多く、日本人では比較的少ないが、日本人のゲノムにも二重瞼形成に関与する遺伝子は存在する。
この点についてTIMC仮説では、細胞内に存在する「形質形成プログラム」をコンピュータの“復元プログラム”に例え、iPS細胞由来エクソソームのマイクロRNAがそのプログラムを再起動させた可能性を提示している。
本仮説では、福富氏の眼瞼変化を「若返り」ではなく、初期胚期に起こる形質決定プロセスの再現(re-activation)として捉えている。
すなわち、受精後4〜7日の胚盤胞期において、胚性幹細胞由来EVsがICMの遺伝子発現に影響を与える現象と類似した分子作用が、成人組織において再び生じた可能性を示唆している。
本仮説は、iPS細胞由来エクソソームが成人組織に対して発生学的プログラムの一部を再活性化しうるという新しい視点を提供するものであり、従来の「若返り」を超えた「形質再構築(phenotypic reprogramming)」の可能性を提起するものである。
【TIMCマイクロRNA新報EVs 2026年4月6日】